Information de sécurité ANSM – Performance de la batterie de la télécommande
Lève-personne mobile – Elévateur de bain Mangar Achimèdes – Mangar International (filiale du groupe Winncare)

L’ANSM a été informée par la société Mangar International, filiale de Winncare, qu’un utilisateur est resté bloqué dans sa baignoire, car le dispositif, en l’occurrence la télécommande, n’a pas permis de sortir l’utilisateur du bain.
Ce risque concerne intervient si la batterie de la télécommande n’est pas correctement entretenue. La batterie intégrée n’est pas remplaçable et sa performance dépend de l’usage et du stockage. Lorsqu’elle ne peut plus tenir la charge, un voyant rouge clignote, indiquant qu’il faut remplacer la télécommande. La durée de vie de la télécommande varie selon l’utilisation.
Aucune blessure n’a été signalée, cependant il existe un risque potentiel que cet incident, dans des cas extrêmes, puisse entraîner des escarres ou une baisse de la température corporelle.
Information de sécurité ANSM – Composant interne du vérin défectueux
Lève-personne mobile Tenor – ArjoHuntleigh AB
(Fabriqués entre le 06 mars et le 28 novembre 2025)
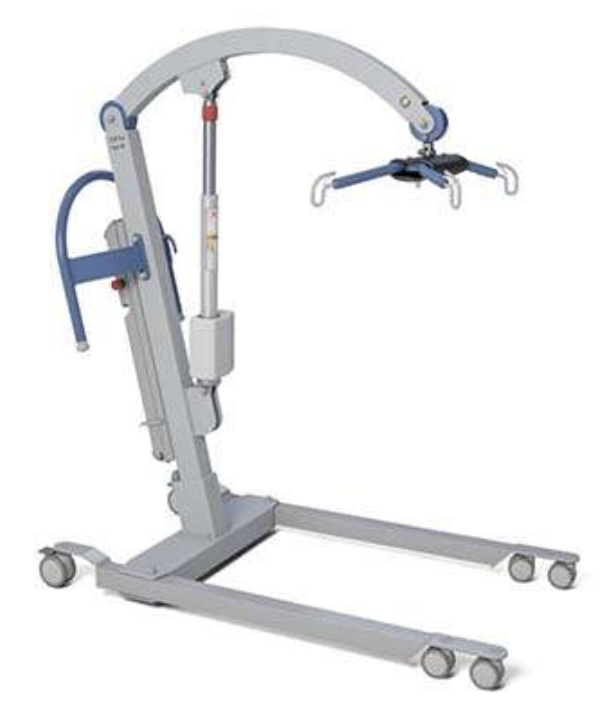
L’ANSM a été informée par la société Arjo qu’une anomalie de fonctionnement a été détectée durant les tests de production finaux en usine.
Il a été confirmé qu’un composant interne du vérin pouvait être défectueux et ne pas présenter la résistance mécanique requise. Dans le cas le plus défavorable, cela pourrait entraîner une perte soudaine de la capacité du vérin à supporter la charge et provoquer un mouvement brusque et incontrôlé du bras de levage vers le bas.
Ce dysfonctionnement n’est pas détectable lors de tests, il ne devient apparent qu’au moment de la défaillance. L’utilisation continue d’un lève‑personne Tenor ayant un vérin défectueux peut exposer les patients et les soignants à un risque. Ils doivent donc être mis en quarantaine sans délai et ne plus être utilisés tant qu’un technicien n’est pas intervenu pour remplacer le vérin.
Information de sécurité ANSM Urgente – Mise à jour de la notice d’utilisation
L’ANSM a été informée par la société Kinetec SAS d’une utilisation non appropriée du pansement Manosplint Cushionfoam pour créer des bandages hermétiques, provoquant ainsi des réactions cutanées.
L’utilisation d’un bandage circulaire peut entraîner un risque de réaction cutanée, notamment lorsque la mousse Manosplint® Cushion est employée pour réaliser une immobilisation circulaire fermée ou pour créer tout type d’environnement cutané occlusif.
Les références de pansement concernées par l’information de sécurité sont :
- M300000027
- M300000028
- M300000029
- M300000030
L’analyse de risque a été révisée afin d’intégrer le risque lié à l’utilisation d’une technique de bandage inappropriée dans la notice.
Parution JORF – Avis de projet tarifaire – Véhicules pour personnes en situation de handicap (VPH) remis en bon état d’usage (RBEU)
L’avis de projet relatif aux tarifs et prix limites de ventes (PLV) au public en euros TTC des véhicules pour personnes en situation de handicap (VPH) remis en bon état d’usage (RBEU) visés au titre IV de la liste prévue à l’article L. 165-1 du code de la sécurité sociale, annoncé dans notre Info du 04 mars 2026, est paru au JORF du 11 mars 2026.
👉 Comme pour tous les avis de projets, nous disposons d’un délai de 20 jours pour solliciter une audition auprès du Comité Economique des Produits de Santé, ce que nous ferons probablement afin d’illustrer, auprès de ses membres qui l’ignorent, ce que peut revêtir concrètement le processus de remise en bon état d’usage.
Information de sécurité ANSM – Rappel de produit et remplacement préventif de la barre d’appui du guidon » VERSO » – Lève-personne mobile – Verticalisateur Verso – Alter Eco Santé

L’ANSM a été informée par la société Alter Eco Santé de la survenue d’un problème ayant déjà fait l’objet d’un précédent avis de sécurité en décembre 2024 (avis R2501761, publié sur le site de l’ANSM le 21 janvier 2025). De nouvelles barres d’appui susceptibles de présenter des défauts de soudure ont depuis été identifiées.
La défaillance constatée correspond à une rupture de soudure située sous la tablette de la barre d’appui. Celle-ci résulte d’une sollicitation intensive et répétée du dispositif du même côté, sans répartition de la charge entre les deux côtés.
Cette défaillance peut entraîner une perte d’équilibre du patient et un risque de chute si le soignant ou l’utilisateur ne parvient pas à la compenser. Elle expose également le soignant ou l’utilisateur aux mêmes risques, lors de la compensation du déséquilibre. Les conséquences potentielles impliquent un risque de blessure tant pour le patient que pour le soignant.
Les 35 produits concernés portent les numéros de série DEV-2024349 jusqu’à DEV-2024384.
La société procède donc au remplacement de la barre d’appui avec la pièce de remplacement.
Parution JORF – Modification des conditions d’inscription – Dispositif d’assistance électrique à la propulsion YOMPER + – ACEKARE
Arrêté du 2 mars 2026 portant modification des conditions d’inscription du dispositif d’assistance électrique à la propulsion YOMPER + de la société ACEKARE inscrit au titre IV de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale paru au JORF du 04 mars 2026.
↪ Date d’entrée en vigueur à compter du 17 mars 2026.
Parution JORF – Modification des conditions d’inscription – Orthèse C-Brace – OTTO BOCK France

Arrêté du 26 février 2026 portant modification des conditions d’inscription de l’orthèse cruropédieuse associée à une articulation hydraulique contrôlée par microprocesseur C-BRACE de la société OTTO BOCK France inscrite au titre II de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale paru au JORF du 03 mars 2026.
↪ Date d’entrée en vigueur à compter du 16 mars 2026.
Parution JORF – Avis rectificatif de l’avis de projet relatif à la tarification – Pieds à restitution d’énergie – Enfant
Avis rectifiant l’avis de projet relatif aux tarifs et prix limites de ventes (PLV) au public en euros TTC des pieds à restitution d’énergie visés au titre II de la liste prévue à l’article L. 165-1 du code de la sécurité sociale paru au JORF du 28 février 2026.
Dans l’avis de projet relatif à la tarification des pieds à restitution d’énergie inscrits au titre II sur la liste des produits et prestations remboursables prévue à l’article L. 165-1 (LPP) du code de la sécurité sociale publié au Journal officiel de la République française n° 43 du 20 février 2026, texte n° 111 (NOR : SFHS2604904V), la ligne :

est remplacée par la ligne suivante :

Parution JORF – Radiation de produits – Pieds à restitution d’énergie – OTTO BOCK France
Arrêté du 23 février 2026 portant radiation de produits sur les références relatives aux petites tailles du pied à restitution d’énergie pour amputation basse de jambe « LO RIDER, réf. 1E57 » de la société OTTO BOCK France inscrites dans le code 2711975 au titre II de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale paru au JORF du 25 février 2026.
Parution JORF – Révision de nomenclature – Grand appareillage orthopédique (GAO)
Arrêté du 19 février 2026 modifiant l’arrêté du 4 décembre 2024 portant révision de la nomenclature du grand appareillage orthopédique (GAO) au titre II de la liste prévue à l’article L. 165-1 (LPP) du code de la sécurité sociale paru au JORF du 24 février 2026.