Parution au JORF – Radiation de produits
Autocontrôle du glucose interstitiel, forfait init + forfait mensuel, DEXCOM – DEXCOM G6
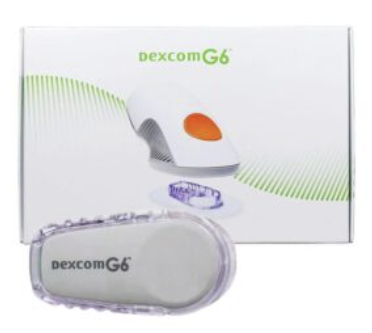
Arrêté du 26 mars 2026 portant radiation de produits au titre I de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale paru au JORF du 31 mars 2026.

↪ Date d’entrée en vigueur à compter du 13 avril 2026.
Parution au JORF – Modification des conditions d’inscription
Système de mesure en continu du glucose interstitiel DEXCOM ONE + de la société DEXCOM France
Arrêté du 24 mars 2026 portant modification des conditions d’inscription du système de mesure en continu du glucose interstitiel DEXCOM ONE + de la société DEXCOM France inscrit au titre I de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale paru au JORF du 26 mars 2026.
↪ Date d’entrée en vigueur à compter du 08 avril 2026.
Parution au JORF – Modification des conditions d’inscription – Système de boucle semi-fermée dédié à la gestion automatisée du diabète de type I CONTROL IQ – TANDEM DIABETES CARE et DEXCOM G7 – DEXCOM France
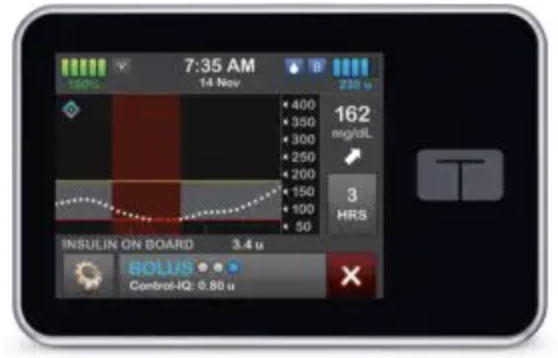
Arrêté du 25 février 2026 portant modification des conditions d’inscription du système de boucle semi-fermée dédié à la gestion automatisée du diabète de type I CONTROL IQ de la société TANDEM DIABETES CARE inscrit au titre I de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale et modification des conditions d’inscription du capteur DEXCOM G7 de la société DEXCOM France associé à une boucle semi-fermée au titre I de la liste susvisée paru au JORF du 27 février 2026.
↪ Date d’entrée en vigueur à compter du 12 mars 2026.
Information de sécurité ANSM Urgente – Systèmes de pompe à insuline MiniMed Paradigm, MiniMed 600 et MiniMed 700 – Medtronic
Positionnement de la pompe par rapport au site de perfusion
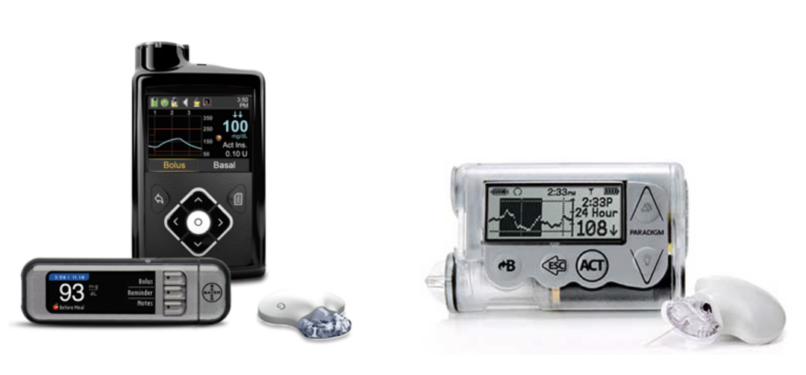
L’ANSM a été informée par la société Medtronic MiniMed de la diffusion d’une information de sécurité urgente concernant les pompes à insuline Paradigm, MiniMed 640G, 740G et 780G.
Lors de tests qualité effectués sur ces pompes à insuline, le fabricant a constaté que la quantité d’insuline administrée pouvait varier en fonction du positionnement de la pompe vis-à-vis du site d’insertion du cathéter :
- Si la pompe est placée au-dessus du site d’insertion, il existe un risque d’administration excessive d’insuline ;
- Si la pompe est placée au-dessous du site d’insertion, il existe un risque d’administration insuffisante d’insuline.
Ce phénomène peut entraîner des variations de la glycémie (hypoglycémie ou hyperglycémie), particulièrement chez les patients les plus sensibles à l’insuline ou nécessitant de faibles doses quotidiennes.
À ce jour, aucun incident lié à ce phénomène n’a été rapporté en France.
Parution au JORF – Avis tarifaire – Capteurs de mesure du glucose interstitiel DEXCOM G6
Avis relatif à la tarification des capteurs de mesure du glucose interstitiel DEXCOM G6 associés à une boucle semi-fermée visés à l’article L. 165-1 du code de la sécurité sociale paru au JORF du 20 février 2026.

Parution au JORF – Inscription de produit, modification de produit et avis tarifaire
Arrêté du 22 janvier 2026 portant :
Modification des conditions d’inscription du système de boucle semi-fermée dédié à la gestion automatisée du diabète de type I OMNIPOD 5 de la société INSULET inscrit au titre I de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale
Modification des conditions d’inscription du système de mesure du glucose interstitiel DEXCOM G6 de la société DEXCOM France associé à une boucle semi-fermée au titre I de la liste susvisée
Inscription du système de mesure du glucose interstitielDEXCOM G7 de la société DEXCOM France associé à une boucle semi-fermée au titre I de la liste susvisée paru au JORF du 27 janvier 2026.
Parution au JORF – Radiation de produit – Système de mesure en continu du glucose interstitiel, DEXCOM, DEXCOM ONE : kit d’initiation, capteur, transmetteur, récepteur
Arrêté du 21 janvier 2026 portant radiation de produits au titre I de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale paru au JORF du 23 janvier 2026.

↪ Entrée en vigueur de l’arrêté à compter du 04 février 2026.
Information de sécurité ANSM Urgente – Appareil de mesure de glucose en continu – Application Dexcom G6 Android CGM version 1.15.0 – Dexcom Inc
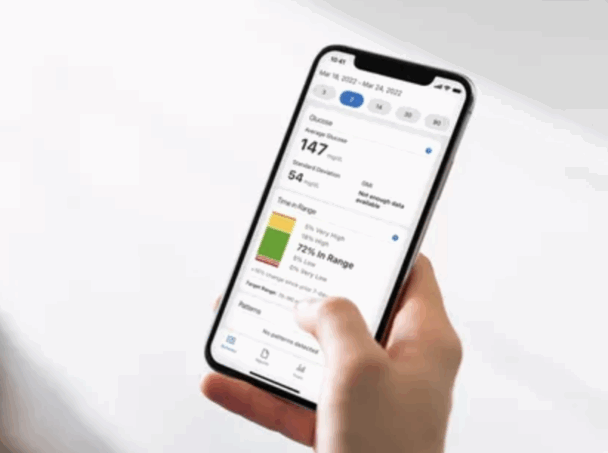
L’ANSM a été informée par la société Dexcom de l’identification d’un dysfonctionnement pouvant affecter les patients en France utilisant un smartphone verrouillé TeDi (Samsung A15 fourni par les Prestataires de Santé à Domicile) comme dispositif d’affichage de l’application Dexcom G6 pour Android, version 1.15.0.
Le smartphone peut ne pas émettre d’alertes sonores ou vibratoires, bien que les alertes visuelles demeurent pleinement opérationnelles. Cette absence de signal sonore ou vibratoire peut empêcher l’utilisateur de détecter une situation d’hypo- ou d’hyperglycémie.
Ce problème ne concerne que les utilisateurs en France équipés d’un smartphone TeDi verrouillé avec l’application G6 version 1.15.0.
Dexcom a déployé une mise à jour à distance des paramètres du téléphone pour corriger ce dysfonctionnement.
Information de sécurité ANSM Urgente – Rappel de plusieurs lots de capteurs
Appareils de mesure du glucose en continu – Capteur FreeStyle Libre 3 et capteur FreeStyle Libre 3 Plus – Abbott Diabetes Care Ltd

L’ANSM a été informée par la société Abbott Diabetes Care Inc. du rappel de plusieurs lots de capteurs FreeStyle Libre 3 et FreeStyle Libre 3 Plus, utilisés soit avec l’application FreeStyle libre 3 (sur smartphone) soit avec l’application mylife CamAPS FX, incluse dans le système de boucle semi-fermée de la pompe à insuline mylife YpsoPump. Aucune autre référence de capteur FreeStyle n’est impactée.
Ce rappel fait suite à des signalements de capteurs ayant fourni des mesures trop basses du taux de glucose, pouvant entraîner des décisions thérapeutiques inadaptées et présenter un risque sérieux pour la santé des patients diabétiques.
Les utilisateurs ont été invités à vérifier si leurs capteurs font partie des lots concernés en se rendant sur : www.FreeStyleCheck.com
↪ Le numéro de série est indiqué sur la boîte ou dans l’application.
Le cas échéant, les patients ne doivent pas utiliser un capteur concerné par le défaut et sont invités à le jeter. Ils doivent recourir à une autre méthode de mesure de glycémie le temps de se procurer un autre capteur non concerné par le défaut.
Il est rappelé qu’en cas de doute entre la mesure affichée et les symptômes ressentis, il est recommandé d’effectuer une vérification à l’aide d’un lecteur de glycémie capillaire.
Parution au JORF – Modification des conditions d’inscription
Capteur de mesure du glucose interstitiel FREESTYLE LIBRE 2 PLUS associé à une boucle semi-fermée – ABBOTT France

L’arrêté du 28 octobre 2025, qui prévoyait initialement une attribution d’au maximum 25 capteurs par patient et par an, a été modifié. Le nouveau texte de l’arrêté du 24 novembre 2025 paru au JORF du 26 novembre 2025 fixe désormais cette attribution à 25 capteurs par an et par patient.
↪ Entrée en vigueur de l’arrêté à compter du 09 décembre 2025.