
L’ANSM a été informée par la société R82 A/S de la mise en œuvre d’une procédure de sécurité recommandée concernant les dispositifs mentionnés dans le tableau, afin de garantir la poursuite de leur utilisation en toute sécurité.
À la suite d’un faible nombre de retours clients, R82 A/S a été informée d’un possible desserrage de certains boulons au niveau des bras porteurs. Si ces boulons ne sont pas correctement serrés, cela peut entraîner une oscillation du châssis ou une rupture de l’assemblage boulonné, et représenter un risque pour le dispositif et l’utilisateur. Afin de prévenir tout incident, la société recommande de resserrer les boulons et les écrous des assemblages concernés selon la procédure de resserrage transmise. Celle-ci devra être effectuée sur les 8 points identifiés sans utilisateur dans le dispositif.
Parution JORF – Renouvellement et modification des conditions d’inscription – Denrées alimentaires destinées à des fins médicales spéciales pour nutrition orale de la gamme DEKAS de la société ALVEOLUS MEDICAL
Arrêté du 27 janvier 2026 portant modification des conditions d’inscription des denrées alimentaires destinées à des fins médicales spéciales pour nutrition orale de la gamme DEKAS de la société ALVEOLUS MEDICAL au titre I de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale paru au JORF du 30 janvier 2026.
↪ Entrée en vigueur de l’arrêté à compter du 12 février 2026.
Parution JORF – Renouvellement et modification des conditions d’inscription
Denrées alimentaires destinées à des fins médicales spéciales pour nutrition entérale FRESUBIN DB CONTROL de la société FRESENIUS KABI France

Arrêté du 26 janvier 2026 portant renouvellement et modification des conditions d’inscription des denrées alimentaires destinées à des fins médicales spéciales pour nutrition entérale FRESUBIN DB CONTROL de la société FRESENIUS KABI France inscrites au titre I de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale paru au JORF du 28 janvier 2026.
Au titre I de la liste des produits et prestations remboursables, chapitre 1er, section 5, sous-section 2, paragraphe 2, au C « Autres nutriments pour nutrition entérale pour adultes », dans la rubrique « Société FRESENIUS KABI France (FRESENIUS) », la nomenclature du code 1183965 est remplacée comme suit :

↪ Entrée en vigueur de l’arrêté à compter du 10 février 2026.
Parution JORF – Inscription de produit – Système de compression CIRCAID JUXTAFIT ESSENTIALS ARMS de la société MEDI France
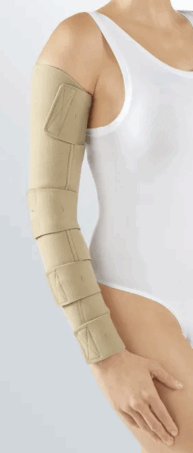
Arrêté du 26 janvier 2026 portant inscription du système de compression CIRCAID JUXTAFIT ESSENTIALS ARMS de la société MEDI France au titre I de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale paru au JORF du 28 janvier 2026.
↪ Date d’entrée en vigueur à compter du 10 février 2026.
La phase de test du téléservice DAP PPC-OAM est désormais terminée. Nous adressons nos remerciements à l’ensemble des entreprises testeuses pour leur participation ainsi que pour leurs précieuses remontées.
À compter du 02 février 2026, tous les distributeurs de PPC et d’OAM pourront utiliser le téléservice et consulter l’avis rendu par le service du contrôle médical sur les DAP PPC-OAM. Vous avez dû recevoir, via la CNAM, un message à cet effet, que vous pouvez consulter ci-dessous.
Information de sécurité ANSM – Lève-personne mobile – Molift Mover 205, Molift Mover 300 et Suspension à 2 points, Suspension à 4 points – Etac A/S
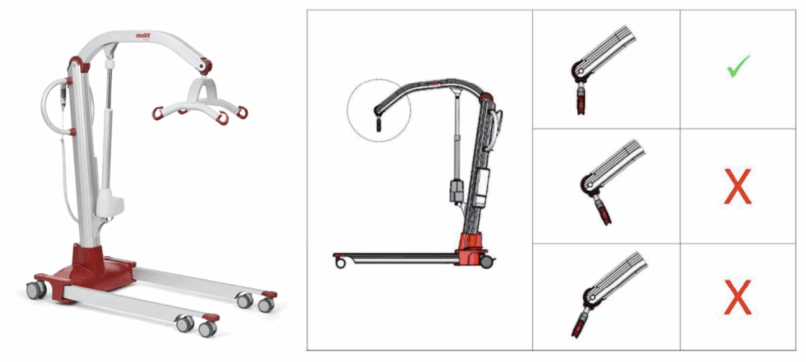
L’ANSM a été informée par la société Etac A/S d’une mesure corrective du Lève-personne mobile – Molift Mover 205, Molift Mover 300 et Suspension à 2 points, Suspension à 4 points.
Il a été constaté que lors de l’assemblage et de l’essai de charge d’un Molifit Mover 300, le boulon de montage de la barre de levage s’est cassé. Suite à une enquête plus approfondie, il a été établi que le défaut se produisait en raison d’une déformation des matériaux impliqué entre la barre de levage et le bras du Molift Mover.
Une telle déformation peut entraîner une mobilité limitée de l’articulation, empêchant ainsi le bon fonctionnement de l’équipement. La défaillance du boulon provoquera la chute de la suspension et, par conséquent, celle du patient, pouvant occasionner des blessures modérées.
Afin de réduire le risque de nouveaux incidents, des unités de remplacement sont proposées pour tous les produits potentiellement concernés. L’utilisation continue est sûre tant que la barre de levage peut se déplacer librement et reste verticale pendant le cycle de levage avec ou sans charge. Les composants des unités défectueuses (Mover 205 et Mover 300) seront progressivement remplacées dans les prochains mois.
Parution au JORF – Inscription de produit, modification de produit et avis tarifaire
Arrêté du 22 janvier 2026 portant :
Modification des conditions d’inscription du système de boucle semi-fermée dédié à la gestion automatisée du diabète de type I OMNIPOD 5 de la société INSULET inscrit au titre I de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale
Modification des conditions d’inscription du système de mesure du glucose interstitiel DEXCOM G6 de la société DEXCOM France associé à une boucle semi-fermée au titre I de la liste susvisée
Inscription du système de mesure du glucose interstitielDEXCOM G7 de la société DEXCOM France associé à une boucle semi-fermée au titre I de la liste susvisée paru au JORF du 27 janvier 2026.
Point de situation sur les difficultés de facturation
À la suite de la mise en œuvre de la réforme des fauteuils roulants, vous avez été nombreux à nous faire remonter des difficultés importantes, tant sur les rejets de facturation que sur l’interprétation des nouvelles règles par les Caisses. Comme annoncé, nous avons alerté la CNAM sur les problématiques majeures rencontrées, sur la base de vos signalements (n’hésitez pas à continuer à nous les transmettre)
Vous trouverez ci-dessous un point de synthèse des éléments abordés lors de la réunion organisée par la CNAM à ce sujet et en particulier trois difficultés majeures :
1. PÉRIODE DE TRANSITION
Une part significative des rejets constatés concerne des facturations réalisées pour les dossiers en cours avant le 1/12/25 avec des codes LPP de l’ancienne nomenclature, au motif de la radiation de ces codes, alors même que ces facturations relèvent de la période transitoire prévue par les textes.
↪︎ La CNAM valide le fait que cette période de transition doit être respectée. Une consigne a été transmise aux CPAM afin qu’elles acceptent effectivement les termes de la nomenclature prévus par l’article 2 de l’arrêté.
2. RENOUVELLEMENT À L’IDENTIQUE
Les rejets observés sont principalement liés :
– Aux codes LPP différents (ancienne/nouvelle nomenclature) pour un même VPH
– À des demandes de pièces justificatives (fiche d’évaluation, fiche de préconisation), alors que celles-ci ne sont pas exigibles dans le cadre d’un renouvellement à l’identique.
↪︎ Les règles ont été rappelées par la CNAM à l’ensemble des Caisses afin d’éviter ces situations.
💡 Cependant, pour attester du caractère identique du VPH, il est demandé de :
– Fournir la facture de l’ancien fauteuil ou l’ancienne fiche de mesures
– Détailler les caractéristiques du fauteuil précédent (photo non exigible)
3. LOCATION DE COURTE DUREE (LCD)
Les outils informatiques de certaines mutuelles n’étant pas correctement paramétrés, un reste à charge « artificiel » est systématiquement généré : les mutuelles prennent en charge la part OCAM sur le tarif LPP et assimilent le différentiel avec le PLV à un dépassement d’honoraires.
↪︎ Il nous a été confirmé qu’il s’agit d’un problème purement technique de paramétrage, la réglementation imposant aux mutuelles la prise en charge intégrale de la location. Une correction est annoncée, même si aucun calendrier précis n’a pu être communiqué à ce stade.
4. AUTRES INFORMATIONS
- Téléservice DAP
- Départements 59, 63 et 33 : il est important de recourir au téléservice mis en place. Un point d’étape devrait être réalisé en février en vue de son extension sur l’ensemble du territoire.
- Pour les PSAD hors départements test, n’attendez pas la généralisation du système et anticipez votre future connection à AmeliPro en vous équipant de cartes CPE.
↪︎ Consultez, pour mémoire, notre info dédiée comportant les informations utiles.
- Documents types
- Deux nouveaux modèles de documents types devraient être mis à disposition dans les prochains jours :
- Certification de validation de l’essai
- Certificat d’aptitude à la conduite (FRE, FREV, FREV, SCO)
- Un modèle de devis ou tout au moins un document précisant les éléments devant impérativement figurer sur le devis pourrait également été proposé ultérieurement.
- Au regard du caractère incomplet voire inexact de la circulaire diffusée auprès des caisses et des pratiques hétérogènes de celles-ci, nous avons demandé à la CNAM qu’elle puisse élaborer un document de référence recensant précisément :
- les pièces justificatives attendues par catégorie de dispositif ;
- les documents requis pour les DAP et pour les factures ;
- les exigences en matière de prescription.
La Caisse ne s’est toutefois pas formellement prononcée sur la mise à disposition d’un tel document.
⚠️ Contrôle actif de la facturation : la CNAM nous a informés de l’engagement de procédures de contrôle très rigoureuses de la facturation. Celles-ci sont engagées sous la mention « contrôle aléatoire », retardant la validation des règlements.
💡 BON À SAVOIR ! EN BREF …
1 – Forfaits PAP : La CNAM a fermement confirmé que les forfaits PAP n’ont pas vocation être facturés en une seule fois de manière systématique : la facturation doit se faire au réel, en une ou plusieurs fois selon les adjonctions apposées. Et ce, indépendamment des injonctions de certaines caisses ou de quelques fournisseurs. Un rappel en ce sens a été effectué.
2 – Forfaits SAV :
a – Les règles relatives aux forfaits PAP s’appliquent également aux forfaits SAV qui n’ont pas vocation à être facturés en intégralité s’il n’y a pas de besoin. La règle est la facturation au réel.
b – Forfait SAV et AAP : la question de la possibilité d’utiliser le SAV 2 pour les AAP a été posée. Ce n’est pas possible en l’état. La DSS va étudier la question. Il est rappelé que le forfait SAV n’a pas à être prescrit.
3 – En cas de Dépassement du PLV ou de supplément esthétique non justifié, la DAP est rejetée globalement : il convient alors d’en établir une nouvelle.
4 – Forfait MAD : la CNAM confirme qu’il n’a pas à être prescrit : une information en ce sens sera renvoyée aux caisses.
5 – Forfait de livraison : en revanche, celui-ci doit être prescrit. Il semblerait que les caisses exigent de plus en plus fréquemment que la prescription soit justifiée par le prescripteur, indiquant que l’usager ne peut se déplacer chez le distributeur.
6 – Règles de cumul : la justification du cumul doit être expressément indiquée sur la prescription.
7 – Ligne sur devis
a – Adjonctions : Toute demande d’adjonctions sur devis sans justification de compensation du handicap conduit à un rejet.
b – VPH non agréés Cerah : la demande sur devis ne pourra a priori concerner que des VPH agréés par le Cerah. Par exemple, pour un FRMS dont une seule référence est agréée, il ne sera pas posssible de faire une demande sur un autre modèle. Ce point semble devoir être reconfirmé par la DSS.
8 – Location de transition : la nécessité de créér un « format » de LCD spécifique aux patients dans l’attente de la délivrance de leur fauteuil définitif a été rappelée une nouvelle fois.
Vous pourrez retrouver ces éléments et de nombreux autres, dans nos FAQ.
Nous sommes pleinement conscients de l’impact de ces problématiques, de la lourdeur de ce dispositif et des retards de règlements sur vos entreprises. Nous allons être prochainement reçus au cabinet de la Ministre : nous ne manquerons pas de l’alerter sur les conséquences de ces difficultés.

Arrêté du 20 janvier 2026 portant renouvellement d’inscription et modification des conditions d’inscription du pied à restitution d’énergie de classe III VARI-FLEX de la société ÖSSUR France inscrit au titre II de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale paru au JORF du 22 janvier 2026.
↪ Date d’entrée en vigueur à compter du 04 février 2026.
Parution JORF – Inscription de produit – Pied à restitution d’énergie de classe I BREEZE de la société ÖSSUR Europe
Arrêté du 20 janvier 2026 portant inscription du pied à restitution d’énergie de classe I BREEZE de la société ÖSSUR Europe au titre II de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale paru au JORF du 22 janvier 2026.
↪ Date d’entrée en vigueur à compter du 04 février 2026.
Parution JORF – Inscription de produit – Pied à restitution d’énergie pour amputation basse de jambe FLEX-SYMES de la société ÖSSUR France

Arrêté du 19 janvier 2026 portant inscription du pied à restitution d’énergie pour amputation basse de jambe FLEX-SYMES de la société ÖSSUR France au titre II de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale paru au JORF du 21 janvier 2026.
↪ Date d’entrée en vigueur à compter du 03 février 2026.
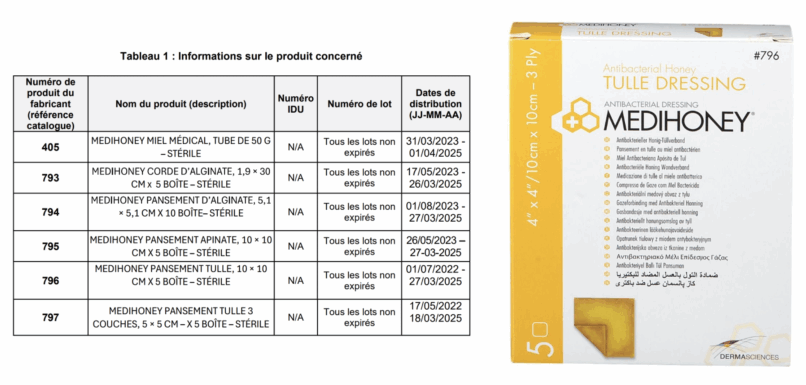
L’ANSM a été informée par la société Integra LifeSciences d’un rappel volontaire des produits Medihoney® Plaies et brûlures énumérés dans le tableau 1, en raison de défaillance d’emballage pouvant compromettre la barrière stérile.
L’investigation a déterminé que ce problème potentiel pourrait affecter l’ensemble de la gamme de produits stériles MediHoney®. Le rappel est donc étendu à toute la gamme de produits stériles MediHoney®. Selon l’évaluation des risques pour la santé (HHE) réalisée à ce sujet, le danger potentiel est une infection si un produit non stérile est utilisé sur un patient.
De plus, l’incapacité d’utiliser le dispositif en raison de défauts d’emballage peut causer des désagréments à l’utilisateur et prolonger ou retarder la procédure. Aucune conséquence à long terme sur la santé n’est attendue en raison de ces problèmes potentiels.
Si vous avez déjà utilisé les produits concernés par ce rappel et que les soins opératoires standard ont été suivis, aucun suivi supplémentaire d’un patient est nécessaire.