Parution JORF – Avis rectificatif de l’avis de projet relatif à la tarification – Pieds à restitution d’énergie – Enfant
Avis rectifiant l’avis de projet relatif aux tarifs et prix limites de ventes (PLV) au public en euros TTC des pieds à restitution d’énergie visés au titre II de la liste prévue à l’article L. 165-1 du code de la sécurité sociale paru au JORF du 28 février 2026.
Dans l’avis de projet relatif à la tarification des pieds à restitution d’énergie inscrits au titre II sur la liste des produits et prestations remboursables prévue à l’article L. 165-1 (LPP) du code de la sécurité sociale publié au Journal officiel de la République française n° 43 du 20 février 2026, texte n° 111 (NOR : SFHS2604904V), la ligne :

est remplacée par la ligne suivante :

Parution au JORF – Modification des conditions d’inscription – Système de boucle semi-fermée dédié à la gestion automatisée du diabète de type I CONTROL IQ – TANDEM DIABETES CARE et DEXCOM G7 – DEXCOM France
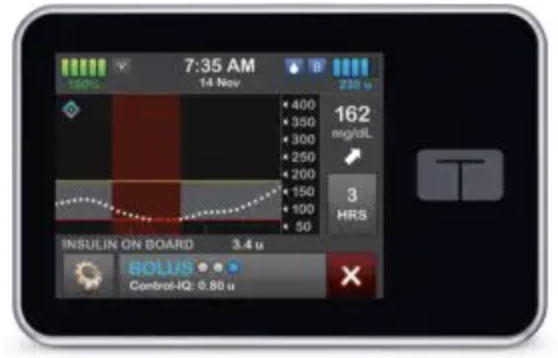
Arrêté du 25 février 2026 portant modification des conditions d’inscription du système de boucle semi-fermée dédié à la gestion automatisée du diabète de type I CONTROL IQ de la société TANDEM DIABETES CARE inscrit au titre I de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale et modification des conditions d’inscription du capteur DEXCOM G7 de la société DEXCOM France associé à une boucle semi-fermée au titre I de la liste susvisée paru au JORF du 27 février 2026.
↪ Date d’entrée en vigueur à compter du 12 mars 2026.
Parution au JORF – Renouvellement d’inscription de produit – Système de nébulisation pneumatique AEROLIGHT/EXTRANEB+ de la société DTF MEDICAL – La Diffusion Technique Française
Arrêté du 23 février 2026 portant renouvellement d’inscription du système de nébulisation pneumatique AEROLIGHT/EXTRANEB+ de la société DTF MEDICAL – La Diffusion Technique Française inscrit au titre I de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale paru au JORF du 26 février 2026.
↪ Date d’entrée en vigueur à compter du 11 mars 2026.
Information de sécurité ANSM Urgente – Systèmes de pompe à insuline MiniMed Paradigm, MiniMed 600 et MiniMed 700 – Medtronic
Positionnement de la pompe par rapport au site de perfusion
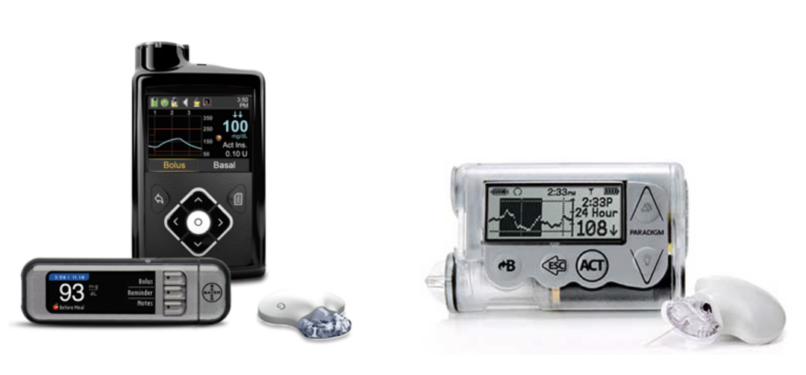
L’ANSM a été informée par la société Medtronic MiniMed de la diffusion d’une information de sécurité urgente concernant les pompes à insuline Paradigm, MiniMed 640G, 740G et 780G.
Lors de tests qualité effectués sur ces pompes à insuline, le fabricant a constaté que la quantité d’insuline administrée pouvait varier en fonction du positionnement de la pompe vis-à-vis du site d’insertion du cathéter :
- Si la pompe est placée au-dessus du site d’insertion, il existe un risque d’administration excessive d’insuline ;
- Si la pompe est placée au-dessous du site d’insertion, il existe un risque d’administration insuffisante d’insuline.
Ce phénomène peut entraîner des variations de la glycémie (hypoglycémie ou hyperglycémie), particulièrement chez les patients les plus sensibles à l’insuline ou nécessitant de faibles doses quotidiennes.
À ce jour, aucun incident lié à ce phénomène n’a été rapporté en France.
Parution JORF – Radiation de produits – Pieds à restitution d’énergie – OTTO BOCK France
Arrêté du 23 février 2026 portant radiation de produits sur les références relatives aux petites tailles du pied à restitution d’énergie pour amputation basse de jambe « LO RIDER, réf. 1E57 » de la société OTTO BOCK France inscrites dans le code 2711975 au titre II de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale paru au JORF du 25 février 2026.
Parution JORF – Révision de nomenclature – Grand appareillage orthopédique (GAO)
Arrêté du 19 février 2026 modifiant l’arrêté du 4 décembre 2024 portant révision de la nomenclature du grand appareillage orthopédique (GAO) au titre II de la liste prévue à l’article L. 165-1 (LPP) du code de la sécurité sociale paru au JORF du 24 février 2026.
Information de sécurité ANSM – Lit médical Essenza 300 – Linet Spol S.R.O

L’ANSM a été informée par la société Linet de la survenue possible d’un coupe-circuit entre les conducteurs du clavier à membrane du contrôleur ACP, susceptible d’entraîner un dysfonctionnement partiel ou total des fonctions électriques du lit. La probabilité d’apparition de ce défaut est toutefois considérée comme très faible. Vous trouverez ci-dessous la référence du lot concerné :

Pour tous les lits Essenza 300 équipés d’un contrôleur ACP issu du lot suspect, le remplacement de cette pièce est requis, et l’ensemble des fonctions électriques du lit devra être vérifié conformément à un protocole qui sera établi à cet effet.
Information de sécurité ANSM Urgente – Table d’examen – Trytable TU2000 – Medkonsult Medical Technology s.r.o
L’ANSM a été informée par la société Medkonsult Medical Technology s.r.o, de la survenue d’un problème relatif à une inclinaison incontrôlée du dossier du fauteuil d’examen, notamment lors de la phase finale de basculement vers la position horizontale. Si ce dysfonctionnement se produit au cours du positionnement du patient, le mouvement brusque du dossier est susceptible d’entraîner des blessures.
Par conséquent, les fauteuils concernés ne doivent pas être maintenus en service, en raison du risque potentiel pour la sécurité des patients. Chaque fauteuil doit faire l’objet d’une vérification afin de déterminer s’il est concerné par ce défaut potentiel et, le cas échéant, la pièce en acier inoxydable dans laquelle s’engage la goupille de verrouillage de position devra être remplacée.
Information de sécurité ANSM – Aides aux soins et à la mobilité – Souris gyroscopique Quha Zono X – Quha Oy

L’ANSM a été informée par la société Quha Oy d’un risque lié à la présence, dans certains dispositifs, d’un composant électronique susceptible d’affecter la charge de la batterie. Dans certaines conditions, le courant de charge pourrait dépasser la valeur maximale spécifiée, susceptible d’entraîner une défaillance de la cellule de batterie et pouvant conduire à une inflammation du dispositif pendant la phase de charge.
Aucun incident ni aucun dommage n’ont été signalés à ce jour dans le cadre de cette action de sécurité (FSCA). La gravité potentielle des conséquences étant jugée élevée, la société met en œuvre une mesure corrective visant à réduire un risque identifié dans le cadre de ses contrôles internes de qualité.
Parution JORF – Avis de projet – Pieds à restitution d’énergie
Avis de projet relatif aux tarifs et prix limites de ventes (PLV) au public en euros TTC des pieds à restitution d’énergie visés au titre II de la liste prévue à l’article L. 165-1 du code de la sécurité sociale paru au JORF du 20 février 2026.