Parution au JORF – Modification de l’arrêté du 23 avril 2026
Systèmes de mesure en continu du glucose interstitiel SIMPLERA SYNC, GUARDIAN 3 et GUARDIAN 4 – MEDTRONIC France
Arrêté du 30 avril 2026 modifiant l’arrêté du 23 avril 2026 portant inscription du système de boucle semi-fermé dédié à la gestion automatisée du diabète de type 1 MINIMED 780G associé au système de mesure en continu du glucose interstitiel SIMPLERA SYNC de la société MEDTRONIC France au titre I de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale et modification des conditions d’inscription du système de boucle semi-fermé dédié à la gestion automatisée du diabète de type 1 MINIMED 780G associé aux systèmes de mesure en continu du glucose interstitiel GUARDIAN 3 et GUARDIAN 4 de la société MEDTRONIC France inscrits au titre I de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale paru au JORF du 04 mai 2026.
Les modifications portent sur les indications d’âge des patients :
Article 1 : Dans l’Article 1er de l’arrêté du 23 avril 2026, dans la rubrique « Système MINIMED 780G associé au système de mesure en continu du glucose interstitiel GUARDIAN 4 », dans le paragraphe « INDICATIONS PRISES EN CHARGE », la mention suivante « enfants âgés d’au moins 2 ans » est remplacée par « enfants âgés d’au moins 7 ans ».
Article 2 : Dans l’Article 2 de l’arrêté du 23 avril 2026, dans la rubrique « Système MINIMED 780G associé au système de mesure en continu du glucose interstitiel SIMPLERA SYNC », le paragraphe « INDICATIONS PRISES EN CHARGE », est remplacé comme suit :
« Patients diabétiques de type 1, adultes et enfants âgés d’au moins 2 ans, dont l’objectif glycémique n’est pas atteint en dépit d’une insulinothérapie intensive bien conduite (dose quotidienne totale d’insuline ≥ 6 unités par jour) par perfusion sous-cutanée continue d’insuline (pompe externe) et d’une autosurveillance glycémique pluriquotidienne (≥ 4/j).»
Information de sécurité ANSM urgente – Fauteuil roulant manuel – Gamme Avantgarde 4 et gamme Zenit – Otto Bock Mobility Solutions GmbH
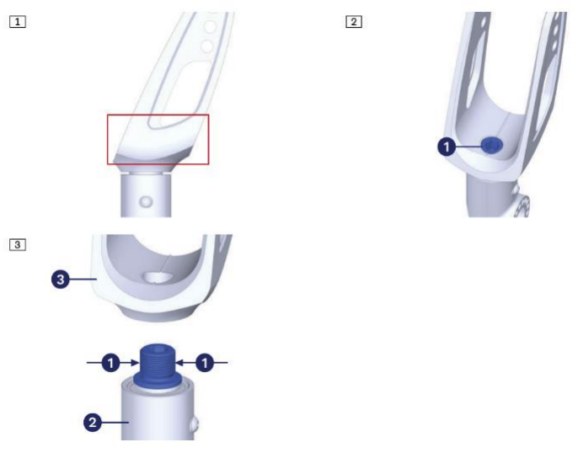
L’ANSM a été informée par la société Otto Bock Mobility Solutions GmbH que des écarts ont été constatés sur les fourches de roue des fauteuils roulants Avantgarde 4 et Zenit, concernant le frein-filet et le couple de serrage de la liaison vissée entre la fourche et le boulon associé. Plus de 80 % des groupes d’assemblage du lot de production identifié sont susceptibles d’être affectés.
La connexion vissée entre la fourche de roue et le boulon de fourche peut se desserrer progressivement et entraîner un décrochage de la fourche si cette défaillance n’est pas détectée. Ce phénomène peut provoquer le basculement du fauteuil roulant. Si des repose-pieds sont installés et non écartés sur le côté, le risque de basculement est réduit car les repose-pieds touchent le sol.
Le desserrage de la connexion vissée sera probablement perçu par l’utilisateur car le dévissage du boulon entraîne une surélévation du cadre du côté concerné et une modification de la position assise. De plus, le fauteuil aura tendance à tirer d’un côté lors de la conduite.
La société a transmis le manuel de service des produits Avantgarde 4 et Zenit afin de permettre la vérification des fauteuils et, le cas échéant, la réalisation des opérations de maintenance.
Information de sécurité ANSM Urgente – Poches nominatives de nutrition parentérale (préparations magistrales) – Baxter Façonnage
RAPPEL DE PRODUITS
Le laboratoire Baxter Façonnage procède, par mesure de précaution, au rappel des Poches nominatives de nutrition parentérale (préparations magistrales) fabriquées le 23 avril 2026 sur le site de Montpellier mentionnées ci-dessous :
- 04 M 6 113 F02 778
- 04 M 6 113 F02 779
- 04 M 6 113 F02 780
- 04 M 6 113 F02 781
- 04 M 6 113 F02 782
- 04 M 6 113 F02 783
- 04 M 6 113 F02 784
- 04 M 6 113 F02 785
Ce rappel, réalisé le 27 avril 2026 en direct auprès des établissement concernés, fait suite à l’identification lors de la lecture quotidienne des prélèvements environnementaux, d’une contamination sur quatre prélèvements.
L’investigation sur l’origine de cette anomalie est en cours. Ce rappel a été effectué en direct auprès des deux établissements concernés. Aucun numéro d’alerte n’a donc été attribué à ce retrait.
Parution JORF – Inscription de produit
Pied prothétique avec articulation de cheville LUNARIS ESSENTIAL – AXILES BIONICS
Arrêté du 27 avril 2026 portant inscription du pied prothétique avec articulation de cheville LUNARIS ESSENTIAL de la société AXILES BIONICS au titre II de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale paru au JORF du 29 avril 2026.
↪ Date d’entrée en vigueur à compter du 12 mai 2026.
Information de sécurité ANSM urgente – Pompe à insuline externe – Système de perfusion Kaleido (avec DBLG1) – ViCentra BV
Conduite à tenir en cas d’hyperglycémie prolongée
L’ANSM a été informée par la société Kaleido d’un rappel de conduite à tenir en cas d’hyperglycémie pour les utilisateurs de la pompe à insuline externe – Système de perfusion Kaleido avec DBLG1 ViCentra BV.
La surveillance continue de la sécurité par la société a mis en évidence une augmentation des hospitalisations liées à des hyperglycémies prolongées, c’est pourquoi elle procède à un rappel des mesures que les utilisateurs doivent prendre en cas d’épisodes d’hyperglycémies prolongées, notamment lorsque l’alarme 15000 s’affiche sur le terminal DBLG1.
ViCentra n’a pas identifié de défaut de fabrication ou de produit comme cause de l’augmentation des hospitalisations. L’analyse a cependant conclu que les utilisateurs, en particulier, les nouveaux utilisateurs, pourraient avoir besoin d’instructions plus claires sur les mesures à prendre en cas d’hyperglycémies prolongées.
Une mise à jour du message affiché avec l’alarme 15000 a été effectuée. Elle est, d’ores et déjà, incluse dans la version 1.18.1 du logiciel DBLG1 et sera installée automatiquement sur votre appareil au cours du mois d’avril 2026. Ce message a pour but de rappeler les mesures à prendre par les utilisateurs.
Information de sécurité ANSM urgente – Ventilateur pour usage à domicile Vivo 45 LS – Breas Medical AB

L’ANSM a été informée par la société Breas Medical AB de la détection d’un défaut lié au firmware affectant un nombre limité de ventilateurs Vivo 45 LS, équipés des versions de firmware 3.2.1 ou 7.2.1, mis en distribution à compter du 23 mars 2026.
Les références concernées sont :
• Dispositifs distribués entre le 23 mars 2026 et le 2 avril 2026
• Numéros de série compris entre 1R070KF et 1R100F9
• Dates de fabrication entre le 13 février 2026 et le 5 mars 2026
• Dispositifs équipés des versions de firmware 3.2.1 ou 7.2.1
• Dispositifs mis à jour le 23 mars 2026 ou après vers la version du firmware 3.2.1 / 7.2.1
Les dispositifs distribués en dehors de cette période ou équipés d’autres versions de firmware ne sont pas concernés.
Dans les dispositifs avec les versions du firmware concernées, le traitement en ventilation en volume contrôlé (VCV, VCV-SIMV et VCV-MPV) peut, dans certaines conditions de déclenchement, entraîner une réduction significative du volume courant délivré en dessous de la valeur réglée. Les dispositifs et les versions du firmware distribués antérieurement ou ultérieurement ne sont pas concernés par ce problème.
Ce dysfonctionnement ne peut survenir que lors d’une thérapie VCV active et peut être déclenché après l’acquittement d’une alarme de déconnexion ou d’une alarme de pression haute, ou après certaines séquences marche/arrêt. Lorsque cette condition est déclenchée, le dispositif restera dans un état de volume courant faible et continuera de déclencher des alarmes. La condition entraînera une alarme de pression basse et peut également déclencher, des alarmes de Vti bas, de volume minute inspiré faible et d’obstruction. Les modes de ventilation en pression ne sont pas concernés par ce dysfonctionnement.
Le problème identifié a été corrigé dans la version du firmware 3.2.3 / 7.2.3 publiée le 16 avril 2026. Breas n’a connaissance d’aucun incident signalé lié à ce problème.
Parution au JORF – Inscription de produit et modification des conditions d’inscription de produit
Système de mesure en continu du glucose interstitiel SIMPLERA SYNC – MEDTRONIC France
Arrêté du 23 avril 2026 portant inscription du système de boucle semi-fermé dédié à la gestion automatisée du diabète de type 1 MINIMED 780G associé au système de mesure en continu du glucose interstitiel SIMPLERA SYNC de la société MEDTRONIC France au titre I de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale paru au JORF du 28 avril 2026.
Système de boucle semi-fermé dédié à la gestion automatisée du diabète de type 1 MINIMED 780G
Arrêté du 23 avril 2026 portant modification des conditions d’inscription du système de boucle semi-fermé dédié à la gestion automatisée du diabète de type 1 MINIMED 780G associé aux systèmes de mesure en continu du glucose interstitiel GUARDIAN 3 et GUARDIAN 4 de la société MEDTRONIC France inscrits au titre I de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale paru au JORF du 28 avril 2026.
Information de sécurité ANSM – Appareils de mesure du glucose en continu – lecteur
Mise à jour de l’application Dexcom G7 iOS CGM App et Application Dexcom ONE+ iOS CGM App – Dexcom Inc
L’ANSM a été informée par la société Dexcom Inc de l’obligation pour les patients utilisateurs de certains appareils de mesure en continu de la glycémie, de mettre à jour l’application présente sur leur smartphone. Cette mise à jour obligatoire concerne les applications des récepteurs Dexcom G7 iOS/G7 Watch iOS et Dexcom ONE+ iOS.
En effet, une erreur logicielle a été identifiée dans ces applications, pouvant entrainer un risque de retardement des alarmes/alertes de glycémie dont les conséquences peuvent conduire à des hyperglycémies ou hypoglycémies non détectées.
Les patients concernés sont directement informés par le fabricant qu’ils doivent mettre à jour leur application sur leur smartphone à la version la plus récente, par le biais de notifications reçues dans l’application et par un courrier du fabricant (ci-dessous).
Cette mise à jour doit être faite au plus tard le 30 avril 2026.
Après cette date, les versions 2.11.2 et antérieures pour l’application Dexcom G7 iOS/G7 Watch iOS, et les versions 1.6 et antérieures pour l’application Dexcom ONE+ iOS, ne pourront plus être utilisées. Les patients n’ayant pas mis à jour leur application devront effectuer cette mise à jour pour pouvoir de nouveau l’utiliser. Début avril 2026, le fabricant n’avait pas reçu de signalement en lien avec ce problème en France.
Information de sécurité ANSM – Lit médical – Demi-barrières coulissantes de lits Aerys et Aerys Confort – Winncare France
Demi-barrières coulissantes associées aux lits AERYS (AE4) ou AERYS CONFORT (AF3)
L’ANSM a été informée par la société Winncare de risques potentiels liés à l’utilisation des demi-barrières coulissantes, pouvant entraîner des irritations, rougeurs, dermabrasions et/ou des phénomènes de cisaillement de l’épiderme au niveau de la face postérieure des cuisses des résidents.
Ces situations ont été observées lors de la sortie du lit : lorsque la demi-barrière est en position basse, certains résidents prennent appui sur la main courante afin de se relever. Ce contact répété, associé aux frottements liés au mouvement de sortie du lit, peut être à l’origine des effets indésirables précités.
Ces cas concernent principalement des résidents de petite taille, présentant une autonomie suffisante pour sortir du lit sans assistance, et dont les membres inférieurs ne sont pas systématiquement vêtus au moment du lever.
En complément de cette information, la société Winncare a apporté une mise à jour à la notice d’utilisation (référence : 580318, version 26_04_13), laquelle annule et remplace les versions précédemment transmises avec les dispositifs (références : 580318, versions 25_06_19 ou 2026.01.05).
Parution JORF – Inscription de produit – Paire de roues pour fauteuil roulant manuel avec dispositif de freinage intégré DREEFT – MOTION COMPOSITES
Arrêté du 13 avril 2026 portant inscription de la paire de roues pour fauteuil roulant manuel avec dispositif de freinage intégré DREEFT de la société MOTION COMPOSITES au titre IV de la liste des produits et prestations remboursables prévue à l’article L. 165-1 du code de la sécurité sociale paru au JORF du 15 avril 2026.
Réforme Fauteuils Roulants – Mise à jour de la FAQ du Ministère
👉 Vous trouverez ci-dessous la FAQ : Réforme de la prise en charge intégrale des fauteuils roulants mise à jour le 10 avril 2026.
👉 Vous pouvez également vous référer à notre communication du 10 avril 2026, dans laquelle nous vous présentions les éléments de réponse apportés par la CNAM concernant les difficultés de facturation des VPH dans le cadre de la réforme.